چکیده:
در مقاله قبلی ریسمونک به “برهم کنش ذرات با یک میدان خارجی – فیزیک حالت جامد” پرداختیم، با آگاهی از نوع و مقدار نیروهای بین مولکولی می توان حل شدن یا نشدن مواد در یک حلال معین را پیش بینی کرد. در این مقاله کمی بیشتر پیرامون انواع برهم کنش های بین ذره ای و خصوصیات آن ها بحث خواهیم کرد.
بر هم کنش های بین ذره ای ( میان مولکول – مولکول یا یون – مولکول) را به افتخار یک فیزیکدان هلندی، نیروهای وان دروالسی می نامند. این نیروها به چند نوع تقسیم می شوند.
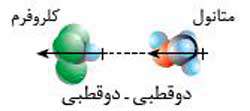
۱- جاذبه دو قطبی – دوقطبی: بین دو مولکول قطبی جاذبه ای از این نوع به وجود می آید. بدین ترتیب که سر مثبت یک مولکول به سر منفی مولکول مجاورش جذب می شود.
- مثال: جاذبه بین مولکول متانول (CH۳OH) با مولکول کلروفرم (CHCl۳)
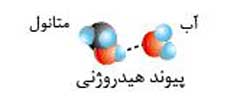
۲- پیوند هیدروژنی: این پیوند نوع خاصی از نیروی دوقطبی- دوقطبی است که بین مولکول های دارای پیوند H-F ,O-H, N-H به وجود می آید.
- مثال: پیوند هیدروژنی میان مولکول های آب و متانول
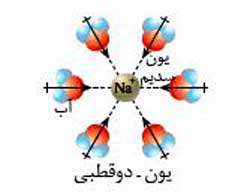
۳- جاذبه یون – دوقطبی: در اثر نیروی جاذبه بین یک یون و یک مولکول قطبی این نیرو به وجود می آید که سبب انحلال ترکیب های یونی در آب (آب پوشی) می شود.
- مثال: جاذبه بین مولکول های آب با یون سدیم
جاذبه یون – دوقطبی از جاذبه دوقطبی – دوقطبی و پیوند هیدروژنی قوی تر و از پیوند یونی ضعیف تر است.
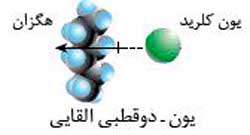
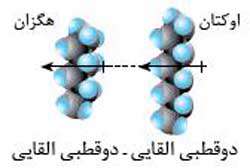
۴- نیروی لاندون یا دوقطبی القایی- دوقطبی القایی: زمانی که ابر الکترونی یک مولکول ناقطبی به دلایل مختلف مانند برخورد الکترون ها و یا حرکت دائم الکترون ها) جا به جا شود و تراکم آن در یک سمت مولکول بیشتر شود و در سوی دیگر کمتر باشد، مولکول دارای بارهای جزئی مثبت و جزئی منفی می شود که به آن دوقطبی القایی می گویند. مولکولی که دارای دوقطبی القایی شده است می تواند روی ابر الکترونی مولکول ناقطبی مجاور خود نیز تاثیر گذاشته و آن را نیز دارای دوقطبی القایی کند. بین دوقطبی های القایی نیرویی به وجود می آید که به آن جاذبه دوقطبی القایی- دوقطبی القایی یا نیروی لاندون می گویند.
- مثال: جاذبه بین اوکتان (C۸H۱۸) و هگزان (C۶H۱۴)
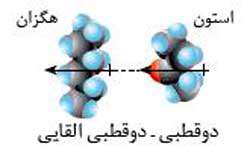
۵- جاذبه دوقطبی – دوقطبی القایی: این نیرو بین یک مولکول قطبی و یک مولکول ناقطبی به وجود می آید و مولکول ناقطبی توسط مولکول قطبی دارای دوقطبی القایی می شود.
- مثال: جاذبه بین مولکول استون (مولکول قطبی) و مولکول هگزان (مولکول ناقطبی)
- مثال: جاذبه میان یون کلرید و مولکول هگزان